Galvanostegia
1 - Panoramica
La galvanostegia, detta anche placcatura, è un procedimento che permette di ricoprire la superficie di un materiale conduttore di elettricità con un altro materiale, anch'esso conduttore. Viene utilizzata principalmente in ambito industriale, per ricoprire oggetti di metallo con altri metalli più nobili o più preziosi. Si realizza immergendo l'oggetto da ricoprire in una soluzione appositamente preparata, che, attraverso l'azione della corrente elettrica, da luogo a una reazione chimica che deposita sull'oggetto uno strato del metallo voluto.
1.1 - I metalli ricoprenti
I metalli più usati per ricoprire sono oro, argento, rame, nichel, cromo e zinco. Molti di questi metalli hanno la proprietà di resistere bene alla corrosione e all'usura del tempo, e sono utilizzati per proteggere l'oggetto e renderlo più duraturo. Alcuni migliorano anche l'aspetto estetico, come il cromo, che da un effetto di metallo lucido (ne sono un esempio i rubinetti dei bagni, che spesso sono in acciaio, metallo opaco, ricoperto di cromo). Altri danno più valore all'oggetto, come oro e argento. In generale i metalli utilizzati per la galvanostegia sono elementi puri, ma talvolta possono essere usate anche leghe di metalli, come l'ottone.
1.2 - Gli oggetti da ricoprire
Non esistono limitazioni sulla forma e le dimensioni degli oggetti da ricoprire. Poichè il processo di ricopertura avviene immergendo l'oggetto in una soluzione liquida, è possibile ricoprire anche parti che con altri metodi, come ad esempio la verniciatura, sarebbe difficile raggiungere. L'unica condizione necessaria per effettuare correttamente il processo è che l'oggetto possa condurre elettricità. In base a questa condizione, si distingue tra galvanostegia e galvanoplastica. La galvanostegia si occupa della placcatura di oggetti conduttori, mentre la galvanoplastica si occupa della ricopertura di oggetti non conduttori.
1.3 - Gli elettrodi e il bagno galvanico
La soluzione liquida nella quale avviene il processo di galvanostegia è detta bagno galvanico. Tale soluzione è tipicamente formata da acqua e dal sale del metallo che si vuole depositare. In alcuni casi, come ad esempio per i metalli pregiati, si utilizzano anche bagni galvanici contenti cianuro, detti bagni al cianuro. Il loro utilizzo è però più complicato, perchè il cianuro è una sostanza altamente velenosa e le industrie che ne fanno uso devono avere speciali autorizzazioni statali e operatori specializzati.
Gli elettrodi sono gli elementi di materiale conduttore immersi nella soluzione che permettono alla corrente elettrica di scorrere attraverso la soluzione e di far avvenire la galvanostegia. L'elettrodo collegato al polo negativo della batteria è detto catodo, e è formato dall'oggetto da ricoprire. L'elettrodo collegato al polo positivo della batteria è detto anodo, e può essere fatto dello stesso metallo che si vuol depositare sull'oggetto da ricoprire, oppure di un altro metallo o graffite.
1.4 - La velocità di deposizione
La velocità di deposizione del metallo sull'oggetto varia in base a molti fattori. I principali sono:
- Concentrazione della soluzione: più la soluzione è concentrata, più la deposizione avviene in fretta. Soluzione più concentrata significa che è stato sciolto più soluto (in questo caso il sale del metallo da depositare, oppure il composto del cianuro) in acqua. Esiste tuttavia un limite alla concentrazione della soluzione, oltre il quale il soluto non si scioglierà più nel solvente, ma si depositerà sul fondo del contenitore, o galleggerà. In tal caso la soluzione è satura: il solvente non è più in grado di sciogliere altro soluto.
- Corrente elettrica: più corrente elettrica scorre negli elettrodi e nella soluzione, più la deposizione avviene rapidamente. Per aumentare la corrente elettrica che scorre nel circuito, si può agire su due fattori: si può aumentare la superficie degli elettrodi, o si può aumentare la corrente che il generatore eroga. Esiste tuttavia una corrente massima che può scorrere nel circuito: superato tale valore, la reazione chimica di galvanostegia non avviene più, perchè l'alta corrente causa altre reazioni chimiche differenti, che prevalgono.
1.5 - Le grandezze in gioco
La galvanostegia si può realizzare per piccoli oggetti, come soprammobili o gioielli, come per grandi strutture, come le carrozzerie delle auto. A seconda delle dimensioni dell'oggetto da ricoprire, le grandezze in gioco cambiano. I bagni galvanici possono avere concentrazioni molto basse o molto alte, a seconda delle sostanze e dei materiali utilizzati, mentre le correnti variano dai milliAmpere per piccoli oggetti, alle decine di ampere per grandi bagni galvanici.
2 - Il procedimento pratico
Il processo di placcatura di un oggetto metallico mediante galvanostegia può essere suddiviso in tre parti: la preparazione della superficie dell'oggeto, il bagno galvanico vero e proprio e infine la pulizia finale della superficie asciutta.
2.1 - La preparazione della superficie: il decapaggio
La galvanostegia richiede che la superficie da ricoprire sia perfettamente pulita. Le impurità infatti non permettono al metallo di depositarsi e di aderire correttamente all'oggetto. Tale operazione è chiamata decapaggio. Possiamo distinguere due fasi:
- Pulizia meccanica: viene effettuata attraverso procedimenti meccanici, come spazzole di metallo o di altro materiale, panni abrasivi, ecc. Ha l'obiettivo di eliminare le impurità maggiori, come ruggine o altri residui di lavorazioni industriali. Lascia tuttavia la superficie non perfettamente pulita, con aloni e altre impurità.
- Pulizia chimica: viene effettuata attraverso reazioni chimiche, principalmente attraverso acidi e basi forti, come acido solforico, acido cloridrico o idrossido di sodio. Poichè l'oggetto è immerso completamente nella liquido pulente, la pulizia è totale e completa.
Le due fasi sono spesso consecutive, ma in alcuni casi si rende necessaria solo la pulizia chimica.
2.2 - Il bagno galvanico
Nel bagno galvanico vengono immersi il catodo, formato dall'oggetto da ricoprire, e l'anodo, formato da un altro oggetto conduttore. I due elettrodi sono collegati a un generatore di corrente. Quando viene acceso il generatore, la corrente inizia a scorrere attraverso gli elettrodi e la soluzione, e il metallo inizia a depositarsi. Dopo un tempo sufficiente, calcolato in base a molti fattori, viene spento il generatore, e viene estratto dalla soluzione l'oggetto ormai ricoperto del metallo.
2.3 - La lavorazione finale
Dopo la galvanostegia, l'oggetto deve essere lavato, per eliminare i residui del bagno galvanico, e eventualmente sottoposto a altri trattamenti, come la lucidatura.
3 - Il processo chimico
La galvanostegia può essere realizzata con svariate soluzioni, che permettono di depositare metalli differenti sugli oggetti sottoposti a bagno galvanico. In questa sezione viene preso in considerazione il caso di una soluzione di solfato di rame, un sale azzurro intenso che può essere reperito nei negozi di giardinaggio e che viene normalmente usato in agricoltura per difendere le piante da funghi, alghe e batteri. Il risultato della galvanostegia con tale prodotto chimico è la deposizione di un sottile straro di rame sull'oggetto immerso nella soluzione. Ricordiamo che il solfato di rame è una sostanza velenosa e va maneggiata con cura.
3.1 - Premessa: il legame ionico
Il legame ionico è un tipo di legame chimico che si realizza tipicamente tra due elementi con una differenza di elettronegatività superiore a 1,9, cioè tra elementi in genere molto distanti tra loro sulla tavola periodica, di solito un metallo e un non metallo. Il risultato di un legame ionico è generalmente un sale, che è appunto l'unione di un metallo con un non metallo. Nel caso dei sali l'elemento con elettronegatività minore (il metallo) cede all'elemento con elettronegatività maggiore (il non-metallo) uno o più elettroni, che si inseriscono negli orbitali del nuovo atomo. A questo punto non esistono più due elementi neutri, ma due ioni: l'atomo che ha ceduto gli elettroni diventa un catione, cioè uno ione carico positivamente, mentre l'atomo che ha ricevuto gli elettroni diventa un anione, cioè un atomo carico negativamente (notiamo che il termine catione e anione si riferiscono a polarità opposte rispetto a catodo e anodo). Catione e anione si attraggono, a causa del segno opposto delle loro cariche, e rimangono uniti, formando il sale. Nel caso del nostro esperimento, il sale è il solfato di rame, che ha composizione CuSO4. Il catione è Cu2+, che cede due elettroni all'anione SO2-4.
3.2 - La corrente
Ricordiamo che la corrente elettrica in un metallo è fisicamente causata da un flusso di elettroni che esce dal polo negativo di un generatore, e entra nel polo positivo del generatore. Il flusso effettivo di elettroni è quindi opposto alla direzione convenzionale normalmente utilizzata in elettrotecnica, che prevede che la corrente esca dal polo positivo del generatore.
3.3 - Il processo
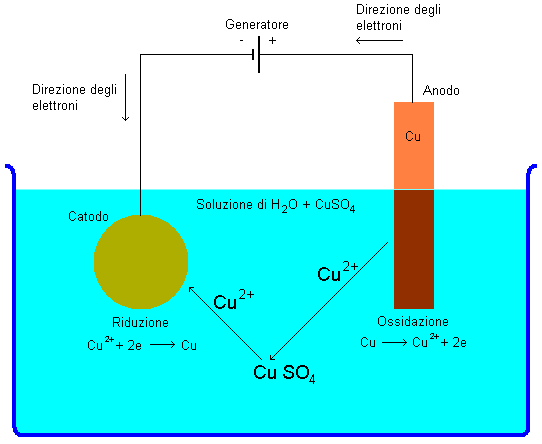
La reazione chimica che causa la galvanostegia è una ossiriduzione, perchè gli atomi di rame in gioco perdono e acquistano elettroni. Quando viene acceso, il generatore cerca di rendere disponibili gli elettroni al catodo, collegato al polo negativo, e di chiamare a se elettroni dall'anodo, collegato al polo positivo. Nel caso del nostro esperimento, il rame dell'anodo perde due elettroni, che si dirigono verso il generatore, e diventa un catione Cu2+. Tale reazione prende il nome di ossidazione. Il solfato di rame CuSO4 sciolto in soluzione rompe il proprio legame ionico, dividendosi nel catione Cu2+ e nell'anione SO2-4. L'anione SO2-4 si lega con il catione Cu2+ che si era formato all'anodo, e si ritrasforma in solfato di rame CuSO4. Il catione Cu2+ che faceva parte del solfato di rame sciolto inizialmente nella soluzione si dirige verso il catodo, dove acquista 2 elettroni, forniti dal generatore, e diventa un elemento neutro, depositandosi sull'oggetto. Tale reazione prende il nome di riduzione.
Di fatto, la reazione comporta un trasferimento di rame: il rame dell'anodo lascia l'elettrodo, e si lega al solfato di rame sciolto in soluzione, mentre il rame del solfato di rame lascia il composto, e si deposita sul catodo. Alla fine della galvanostegia, troviamo questa situazione:
- L'anodo, formato dal rame, si è ridotto (anche se di poco) di dimensioni, perchè ha ceduto degli atomi al solfato di rame.
- La concentrazione del solfato di rame nella soluzione è rimasta invariata, perchè gli atomi di rame che il composto ha ceduto al catodo sono stati sostituiti dagli atomi che ha ricevuto dall'anodo.
- Il catodo, formato dall'oggetto da ricoprire, è aumentato (anche se di poco) di dimensioni, perchè ha acquistato sulla superficie degli atomi di rame.
- Dal punto di vista del generatore, il bilancio di elettroni netto è zero: ha ricevuto due elettroni dall'anodo, ma ne ha ceduti due al catodo.
Copyright 2014-2026 electroimc.com